การระบุเชื้อก่อโรคที่มีปัญหาดื้อยาในประเทศไทยระหว่างปี พ.ศ. 2557 - 2561 โดยใช้ดัชนีทางเลือกยาปฏิชีวนะ
คำสำคัญ:
ดัชนีทางเลือกยาปฏิชีวนะ, การดื้อยาต้านจุลชีพ, เชื้อก่อโรคที่พบบ่อย, ประเทศไทยบทคัดย่อ
ความเป็นมา: สถานการณ์การดื้อยาต้านจุลชีพของเชื้อก่อโรคชนิดหนึ่ง ๆ มักเกี่ยวข้องกับยาปฏิชีวนะหลายชนิดเสมอ ซึ่งยาปฏิชีวนะบางชนิดอาจมีความไวลดลง ในขณะที่ยาปฏิชีวนะชนิดอื่นอาจมีความไวเพิ่มขึ้น ทำให้ยากต่อการประเมินภาพรวมของสถานการณ์การดื้อยา ดัชนีทางเลือกยาปฏิชีวนะ (antibiotic options index, AOI) สามารถแสดงสถานการณ์นี้ในรูปแบบความน่าจะเป็นของการรักษาด้วยยาปฏิชีวนะ
วัตถุประสงค์: เพื่อระบุเชื้อก่อโรคที่เป็นปัญหาโดยใช้ดัชนีทางเลือกยาปฏิชีวนะจากเชื้อก่อโรคที่พบบ่อย 8 ชนิดที่แยกได้จากตัวอย่างเลือดในประเทศไทยระหว่างปี พ.ศ. 2557 - 2561
วิธีวิจัย: รวบรวมข้อมูลความไวต่อยาปฏิชีวนะของเชื้อก่อโรคทั้ง 8 ชนิดที่แยกได้จากตัวอย่างเลือด จากแอนติไบโอแกรมระหว่างปี พ.ศ. 2557 - 2561 ซึ่งเผยแพร่โดยเว็บไซต์ของศูนย์เฝ้าระวังการดื้อยาต้านจุลชีพแห่งชาติ หลังจากนั้นนำมาสร้างดัชนีทางเลือกยาปฏิชีวนะ ซึ่งแทนด้วยสัญลักษณ์ AOIm2 หมายถึงความน่าจะเป็นที่จะมียาปฏิชีวนะที่มีประสิทธิผลอย่างน้อย 2 ชนิดจากตัวเลือกยาปฏิชีวนะทั้งหมด m ชนิด ทั้งนี้ กำหนดให้เชื้อก่อโรคที่เป็นปัญหาคือ เชื้อก่อโรคที่มีค่า AOIm2 ของกลุ่มยาปฏิชีวนะหลัก (1o AOIm2) หรือกลุ่มยาปฏิชีวนะรอง (2o AOIm2) ต่ำกว่าร้อยละ 80
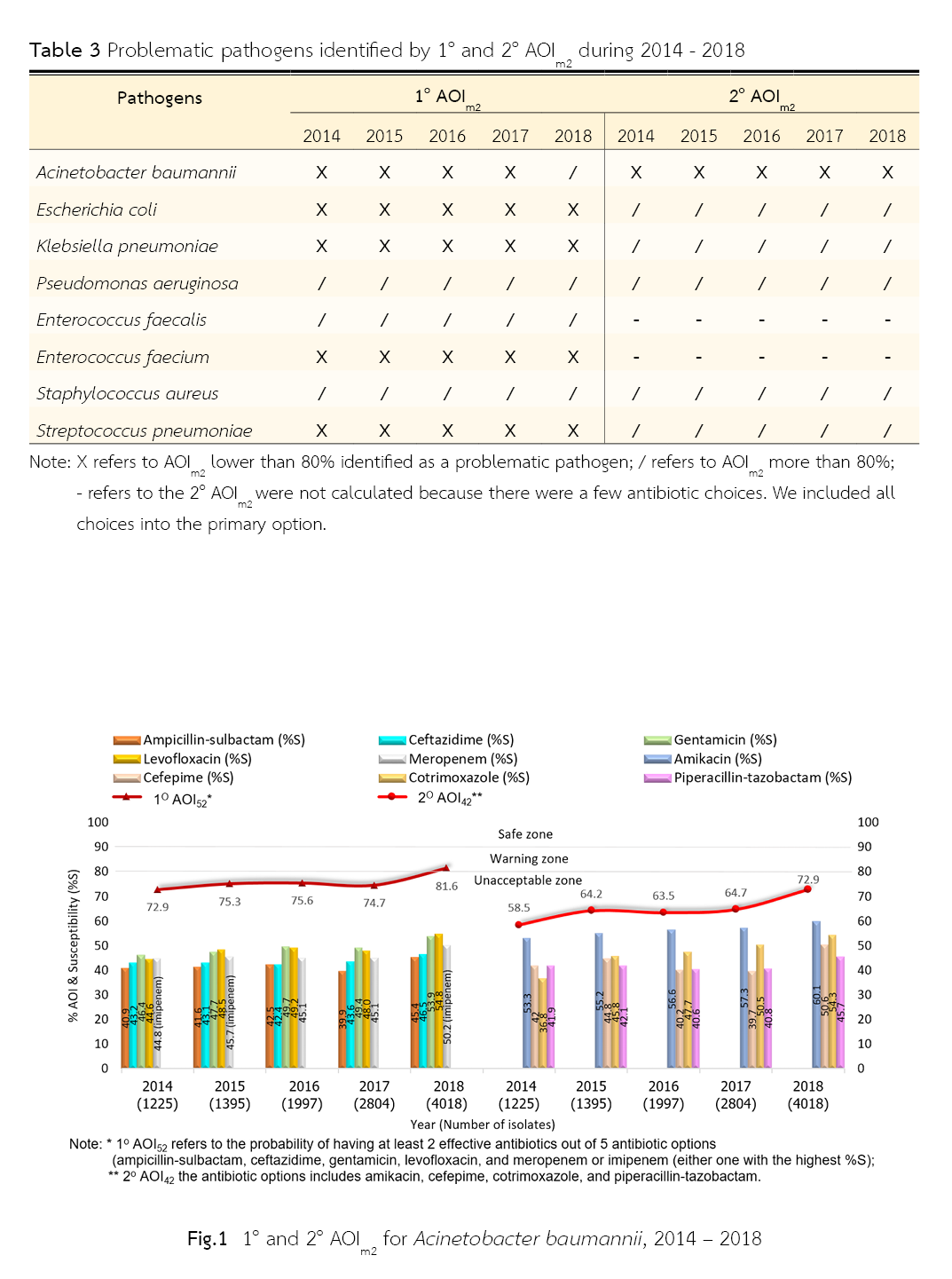
ผลการวิจัย: ระหว่างปี พ.ศ. 2557-2560 พบว่าเชื้อก่อโรคที่มีค่า 1o AOIm2 ต่ำกว่าร้อยละ 80 มี 5 ชนิด ได้แก่ Acinetobacter baumannii, Escherichia coli, Klebsiella pneumoniae, Enterococcus faecium, และ Streptococcus pneumoniae ส่วนใน พ.ศ. 2561 มีเชื้อก่อโรคที่เป็นปัญหาเช่นเดียวกับปี พ.ศ. 2557-2560 ยกเว้น A. baumannii ช่วงระหว่างปี พ.ศ. 2557-2561 เชื้อก่อโรคที่มี 2o AOIm2 ต่ำกว่าร้อยละ 80 มีเพียงชนิดเดียวคือ A. baumannii
สรุปผล: เชื้อก่อโรคที่มีค่า 1o AOIm2 ต่ำกว่าร้อยละ 80 มี 5 ชนิด ระหว่างปี พ.ศ. 2557 - 2560 และ 4 ชนิดในปี พ.ศ. 2561 ส่วนเชื้อก่อโรคที่มีค่า 2o AOIm2 ต่ำกว่าร้อยละ 80 มีเพียงหนึ่งชนิดระหว่างปี พ.ศ. 2557 – 2561
เอกสารอ้างอิง
Kraker MEA, Wolkewitz M, Davey PG, Grundmann H. Clinical impact of antimicrobial resistance in European hospitals: Excess mortality and length of hospital stay related to methicillin-resistant Staphylococcus aureus bloodstream infections. Antimicrob Agents Chemother. 2011;55(4):1598–605.
Cosgrove SE. The relationship between antimicrobial resistance and patient outcomes: mortality, length of hospital stay, and health care costs. Clin Infect Dis. 2006;42(Suppl 2): S82-9.
Dellit TH, Owens RC, McGowan JE, Gerding DN, Weinstein RA, Burke JP, et al. Infectious Diseases Society of America and the Society for Healthcare Epidemiology of America guidelines for developing an institutional program to enhance antimicrobial stewardship. Clin Infect Dis. 2007;44(2):159–77.
Timsit JF, Harbarth S, Carlet J. De-escalation as a potential way of reducing antibiotic use and antimicrobial resistance in ICU. Intensive Care Med. 2014;40:1580–2.
Munoz-Price LS, Quinn JP. Deconstructing the infection control bundles for the containment of carbapenem-resistant Enterobacteriaceae. Curr Opin Infect Dis. 2013;26(4):378–87.
Tacconelli E, Cataldo MA, Dancer SJ, Angelis GD, Falcone M, Frank U, et al. ESCMID guidelines for the management of the infection control measures to reduce transmission of multidrug-resistant Gram-negative bacteria in hospitalized patients. Clin Microbiol Infect. 2014;20 (Suppl 1):1–55.
Doshi P. Speeding new antibiotics to market: A fake fix? BMJ. 2015;350:h1453.
Laxminarayan R, Duse A, Wattal C, Zaidi AKM, Wertheim HFL, Sumpradit N, et al. Antibiotic resistance—the need for global solutions. Lancet Infect Dis. 2013;13(12):1057–98.
Centers for Disease Control and Prevention. US CDC report on antibiotic resistance threats in the United States, 2013 [Internet]. [cited 2020 January 30]. Available from: https://www.cdc.gov/drugresistance/threat-report-2013/pdf/ar-threats-2013-508.pdf
Manomayitthikan T, Borlace GN, Kessomboon N. Development of an antibiotic options index for antibiotic resistance monitoring. Southeast Asian J Trop Med Public Health. 2016;47(6):1288–97.
National Antimicrobial Resistance Surveillance Center of Thailand. Antibiogram [Internet]. [cited 2020 February 10]. Available from: http://narst.dmsc.moph.go.th/antibiograms.html
Clinical and laboratory standards institute. M100 Performance standards for antimicrobial susceptibility testing [Internet]. [cited 2020 January 15]. Available from: https://file.qums.ac.ir/repository/mmrc/CLSI-2018-M100-S28.pdf
National Antimicrobial Resistance Surveillance Center of Thailand. Antibiogram [Internet]. [cited 2020 February 10]. Available from: http://narst.dmsc.moph.go.th/antibiograms/anti2000.pdf
Malathum K. Antibiotic resistance crisis and antibiotic use in Thailand. The report of the situation of drug system 2010:11-15 (in Thai). Available from: http://www.thaidrugwatch.org/download/otherprint/2010_drug_system_report.pdf
Cao J, Song W, Gu B, Mei Y, Tang J, Meng L, et al. Correlation between carbapenem consumption and antimicrobial resistance rates of Acinetobacter baumannii in a university-affiliated hospital in China. J Clin Pharmacol. 2013;53:96-102.
Yang P, Chen Y, Jiang S, Shen P, Lu X, Xiao Y, et al. Association between antibiotic consumption and the rate of carbapenem-resistant Gram-negative bacteria from China based on 153 tertiary hospitals data in 2014. Antimicrob Resist Infect Control. 2018;7:137.
ดาวน์โหลด
เผยแพร่แล้ว
รูปแบบการอ้างอิง
ฉบับ
ประเภทบทความ
สัญญาอนุญาต
ลิขสิทธิ์ (c) 2022 สมาคมเภสัชกรรมโรงพยาบาล(ประเทศไทย)

อนุญาตภายใต้เงื่อนไข Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
ข้อความภายในบทความที่ตีพิมพ์ในวารสารเภสัชกรรมโรงพยาบาลทั้งหมด รวมถึงรูปภาพประกอบ ตาราง เป็นลิขสิทธิ์ของสมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) การนำเนื้อหา ข้อความหรือข้อคิดเห็น รูปภาพ ตาราง ของบทความไปจัดพิมพ์เผยแพร่ในรูปแบบต่าง ๆ เพื่อใช้ประโยชน์ในเชิงพาณิชย์ ต้องได้รับอนุญาตจากกองบรรณาธิการวารสาร (สมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย)) อย่างเป็นลายลักษณ์อักษร
สมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) อนุญาตให้สามารถนำไฟล์บทความไปใช้ประโยชน์และเผยแพร่ต่อได้ โดยอยู่ภายใต้เงื่อนไขสัญญาอนุญาตครีเอทีฟคอมมอน (Creative Commons License: CC) โดย ต้องแสดงที่มาจากวารสาร – ไม่ใช้เพื่อการค้า – ห้ามแก้ไขดัดแปลง, Attribution-NonCommercial-NoDerivatives 4.0 International (CC BY-NC-ND 4.0)
ข้อความที่ปรากฏในบทความในวารสารเป็นความคิดเห็นส่วนตัวของผู้เขียนแต่ละท่านไม่เกี่ยวข้องกับสมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) และบุคลากรในสมาคมฯ แต่อย่างใด ความรับผิดชอบองค์ประกอบทั้งหมดของบทความแต่ละเรื่องเป็นของผู้เขียนแต่ละท่าน หากมีความผิดพลาดใด ๆ ผู้เขียนแต่ละท่านจะรับผิดชอบบทความของตนเอง ตลอดจนความรับผิดชอบด้านเนื้อหาและการตรวจร่างบทความเป็นของผู้เขียน ไม่เกี่ยวข้องกับกองบรรณาธิการ


.png)

