ประสิทธิผลและความปลอดภัยของยาสมุนไพรตำรับเคอร่าต่อลักษณะอาการของโรคโควิด-๑๙ ระยะเริ่มต้น
คำสำคัญ:
โรคโควิด-19, ยาสมุนไพรตำรับเคอร่า, ยาโมลนูพิราเวียร์, การศึกษาแบบสุ่มที่มีกลุ่มควบคุม, การแพทย์ทางเลือก, ตำรับสมุนไพรบทคัดย่อ
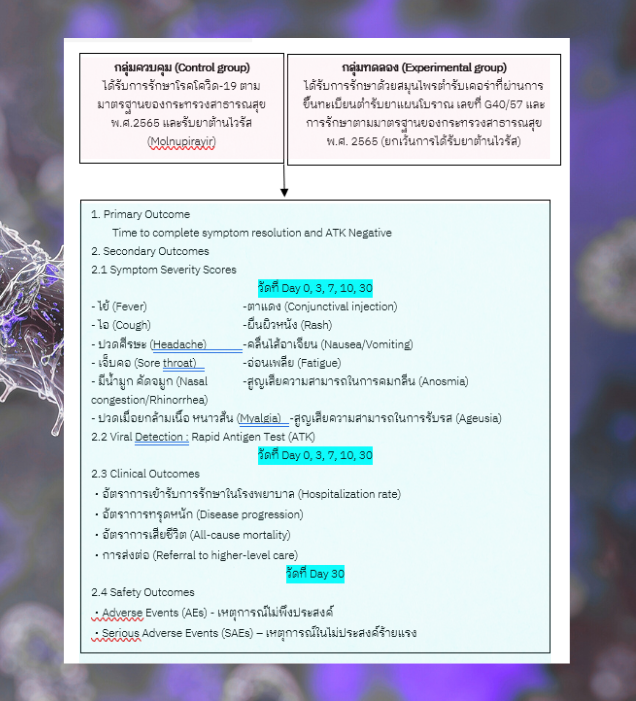
การระบาดของโรคโควิด-19 โดยเฉพาะสายพันธุ์ Omicron ในช่วงต้นปี 2565 ส่งผลกระทบอย่างรุนแรงต่อระบบสาธารณสุขไทย โดยมีผู้ติดเชื้อมากกว่า 4 ล้านราย และผู้เสียชีวิตสะสม 27,899 ราย ยาต้านไวรัสสังเคราะห์มีราคาแพงและมีปริมาณจำกัด ยาสมุนไพรตำรับเคอร่าเป็นทางเลือกที่มีศักยภาพ มีฤทธิ์ยับยั้ง main protease และ RdRp ของเชื้อ SARS-CoV-2 แต่ยังขาดการศึกษาทางคลินิก วัตถุประสงค์: เพื่อเปรียบเทียบประสิทธิผลและความปลอดภัยของยาสมุนไพรตำรับเคอร่ากับยาโมลนูพิราเวียร์ในผู้ป่วยโรคโควิด-19 ระยะเริ่มต้น วิธีการวิจัย: การศึกษาแบบสุ่มที่มีกลุ่มควบคุมที่โรงพยาบาลประชาธิปัตย์ จังหวัดปทุมธานี ระหว่างเดือนกันยายน-พฤศจิกายน 2565 กลุ่มตัวอย่างเป็นผู้ป่วยโรคโควิด-19 จำนวน 230 ราย (อัตราส่วน 1:1) แบ่งเป็นกลุ่มที่รักษาด้วยยาสมุนไพรเคอร่า (n=115) รับประทานวันละ 4 ครั้ง เป็นเวลา 10 วัน และกลุ่มที่รักษาด้วยยาโมลนูพิราเวียร์ (n=115) รับประทาน 800 มก. ทุก 12 ชั่วโมง เป็นเวลา 5 วัน ติดตามผลในวันที่ 3, 7, 10 และ 30 ของการรักษา ประเมินอาการทางคลินิก การตรวจหาเชื้อด้วย ATK และผลข้างเคียง วิเคราะห์ข้อมูลด้วย Independent t-test, Mann-Whitney U test, Chi-square test และ Cochran's Q test (p<0.05)
ผลการวิจัย ยาสมุนไพรตำรับเคอร่ามีประสิทธิผลเทียบเท่ายาโมลนูพิราเวียร์ในการขจัดเชื้อไวรัส (p>0.05) โดยมีข้อได้เปรียบอย่างมีนัยสำคัญในการลดระยะเวลาอาการปวดเมื่อยกล้ามเนื้อ (3.80 vs 4.69 วัน, p=0.036, d=-0.33) และอาการคลื่นไส้ (1.35 vs 2.48 วัน, p=0.012, r=-0.42) อัตราการคงอยู่ในการศึกษาสูง 97.5% ในทั้งสองกลุ่ม ไม่พบผลข้างเคียงร้ายแรง การส่งต่อโรงพยาบาล หรือการเสียชีวิต กลุ่มยาเคอร่ารายงานผลประโยชน์เพิ่มเติมด้านการนอนหลับดีขึ้นและถ่ายอุจจาระอ่อนลง (31.30%) สรุปยาสมุนไพรตำรับเคอร่าเป็นทางเลือกที่มีประสิทธิผลและปลอดภัยในการรักษาโรคโควิด-19 ระยะเริ่มต้น เหมาะสำหรับการบูรณาการเข้าสู่ระบบสาธารณสุข โดยเฉพาะในบริบทที่ต้องการทางเลือกที่เข้าถึงได้ง่ายและมีต้นทุนต่ำ
เอกสารอ้างอิง
Al-Aly, Z., Bowe, B., & Xie, Y. (2022). Long COVID after breakthrough SARS-CoV-2 infection. Nature Medicine, 28(7), 1461–1467. https://doi.org/10.1038/s41591-022-01840-0
Barbara, G., Minucci, G., Cremon, C., Stanghellini, V., & GISCAD. (2022). Prevalence of gastrointestinal symptoms in severe acute respiratory syndrome coronavirus 2 infection: Results of the prospective controlled multinational GI-COVID-19 study. American Journal of Gastroenterology, 117(1), 147–157. https://doi.org/10.14309/ajg.0000000000001541
Benjapholpitak, A., Visitthanon, K., Sawaengdham, T., Thaneerat, T., & Wonarat, K. (2021). Summary report on the use of Andrographis paniculata in the treatment of COVID-19 patients. Journal of Thai Traditional and Alternative Medicine, 19(1), 229-233.
Department of Thai Traditional and Alternative Medicine, Ministry of Public Health, Thailand. (2019). Guidelines for treatment of coronavirus disease 2019 (COVID-19) with Thai traditional medicine formulas and herbal medicine. https://moph.go.th/content/17118/
Department of Disease Control, Ministry of Public Health. (2021, June 4). Coronavirus disease 2019 (COVID-19) situation report No. 518. https://ddc.moph.go.th/viralpneumonia/file/situation/situation-no518-040664.pdf
Department of Medical Services, Ministry of Public Health. (2022, July 11). Clinical practice guidelines for diagnosis, treatment, and prevention of COVID-19 in hospitals for physicians and healthcare personnel (24th ed.). https://covid19.dms.go.th/backend/Content/Content_FIle/Bandner_(Big)/Attach/25650712141035PM_CPG_COVID-19_v.24.1.n_20220711.pdf
Fernandez-de-Las-Penas, C., Rodríguez-Jimenez, J., Fuensalida-Novo, S., Palacios-Cena, M., Gomez-Mayordomo, V., Florencio, L. L., Hernandez-Barrera, V., & Arendt-Nielsen, L. (2021). Myalgia as a symptom at hospital admission by severe acute respiratory syndrome coronavirus 2 infection is associated with persistent musculoskeletal pain as long-term post-COVID sequelae: A case-control study. Pain, 162(12), 2832–2840. https://doi.org/10.1097/j.pain.0000000000002306
Fischer, W. A., Eron, J. J., Holman, W., Cohen, M. S., Fang, L., Szewczyk, L. J., Sheahan, T. P., Baric, R., Mollan, K. R., Wolfe, C. R., Duke, E. R., Azizad, M. M., Borroto-Esoda, K., Wohl, D. A., Coombs, R. W., Loftis, A. J., Alabanza, P., Lipansky, F., & Painter, W. P. (2022). A phase 2a clinical trial of molnupiravir in patients with COVID-19 shows accelerated SARS-CoV-2 RNA clearance and elimination of infectious virus. Science Translational Medicine, 14(628), eabl7430. https://doi.org/10.1126/scitranslmed.abl7430
Herbal Research Institute. (2023). Kera-Acute Toxicity Test (Test Report R6060800201). Department of Medical Sciences.
Jayk Bernal, A., Gomes da Silva, M. M., Musungaie, D. B., Kovalchuk, E., Gonzalez, A., Delos Reyes, V., Martín-Quiros, A., Caraco, Y., Williams-Diaz, A., Brown, M. L., Du, J., Pedley, A., Assaid, C., Strizki, J., Grobler, J. A., Shamsuddin, H. H., Tipping, R., Wan, H., Paschke, A., ... MOVe-OUT Study Group. (2022). Molnupiravir for oral treatment of Covid-19 in nonhospitalized patients. New England Journal of Medicine, 386(6), 509–520. https://doi.org/10.1056/NEJMoa2116044
Lechien, J. R., Chiesa-Estomba, C. M., Place, S., Van Laethem, Y., Cabaraux, P., Mat, Q., Huet, K., Plzak, J., Horoi, M., Hans, S., Rosaria Barillari, M., Cammaroto, G., Fakhry, N., Martiny, D., Ayad, T., Jouffe, L., Hopkins, C., Saussez, S., & COVID-19 Task Force of YO-IFOS. (2020). Clinical and epidemiological characteristics of 1420 European patients with mild-to-moderate coronavirus disease 2019. Journal of Internal Medicine, 288(3), 335–344. https://doi.org/10.1111/joim.13089
Lee, Y., Min, P., Lee, S., & Kim, S. W. (2020). Prevalence and duration of acute loss of smell or taste in COVID-19 patients. Journal of Korean Medical Science, 35(18), e174. https://doi.org/10.3346/jkms.2020.35.e174
Malik, P., Patel, K., Pinto, C., Jaiswal, R., Tirupathi, R., Pillai, S., & Patel, U. (2021). Post-acute COVID-19 syndrome (PCS) and health-related quality of life (HRQoL)—A systematic review and meta-analysis. Journal of Medical Virology, 94(1), 253–262. https://doi.org/10.1002/jmv.27309
Mandelkorn, U., Genzer, S., Choshen-Hillel, S., Reiter, J., Meira e Cruz, M., Hochner, H., Kheirandish-Gozal, L., Gozal, D., & Gileles-Hillel, A. (2021). Escalation of sleep disturbances amid the COVID-19 pandemic: A cross-sectional international study. Journal of Clinical Sleep Medicine, 17(1), 45–53. https://doi.org/10.5664/jcsm.8800
Mao, L., Jin, H., Wang, M., Hu, Y., Chen, S., He, Q., Chang, J., Hong, C., Zhou, Y., Wang, D., Miao, X., Li, Y., & Hu, B. (2020). Neurologic manifestations of hospitalized patients with coronavirus disease 2019 in Wuhan, China. JAMA Neurology, 77(6), 683–690. https://doi.org/10.1001/jamaneurol.2020.1127
Sa-Ngiamsuntorn, K., Suksatu, A., Pewkliang, Y., Thongsri, P., Kanjanasirirat, P., Manopwisedjaroen, S., Charoensutthivarakul, S., Wongtrakoongate, P., Pitiporn, S., Chaopreecha, J., Kongsomros, S., Jearawuttanakul, K., Wannalo, W., Khemawoot, P., Chutipongtanate, S., Borwornpinyo, S., Thitithanyanont, A., & Hongeng, S. (2021). Anti-SARS-CoV-2 activity of Andrographis paniculata extract and its major component andrographolide in human lung epithelial cells and cytotoxicity evaluation in major organ cell representatives. Journal of Natural Products, 84(4), 1261–1270. https://doi.org/10.1021/acs.jnatprod.0c01324
Seetaha, S., Khamplong, P., Wanaragthai, P., Aiebchun, T., Ratanabunyong, S., Krobthong, S., Yingchutrakul, Y., Rattanasrisomporn, J., & Choowongkomon, K. (2022). KERRA, mixed medicinal plant extracts, inhibits SARS-CoV-2 targets enzymes and feline coronavirus. COVID, 2(5), 621–632. https://doi.org/10.3390/covid2050046
Shang, Y.-X., et al. (2022). Adverse effects of andrographolide derivative medications: a review. Frontiers in Pharmacology, 13, 773282. https://doi.org/10.3389/fphar.2022.773282. FrontiersSrathong, P., Butcha, R., , K., Thepaksorn, P., Mongkolsiri, P., Sarakshetrin, A., & Sroisong, S. (2022). Effects of herbal product (Kerra capsule) on clinical features of COVID-19 among home isolation patients in all age groups (A retrospective study). Journal of Positive Psychology & Wellbeing, 6(1), 3161–3170.
Sukati, S., Pikulthong, K., Rerkswattavorn, C., Chanprasertpinyo, W., Thepaksorn, P., Thonglor, N., Boonchu, A., Khamthong, R., Sroisong, S., & Srathong, P. (2022, June). Safety assessment of Kerra formula capsules by oral administration in healthy volunteers: A phase I clinical trial [Conference poster]. Walailak Research Symposium, Walailak University, Thailand.
Thepaksorn, P., Thabsri, K., Denbaes, P. E., Sroisong, S., Srathong, P., & Sukati, S. (2023). Traditional Thai herbal medicine for treating COVID-19. Journal of Applied Pharmaceutical Science, 13(11), 32–39. https://doi.org/10.7324/JAPS.2023.126979
Vetchakorn Osot. (2021). Development of Keera capsule from traditional Thai medicine formula.
World Health Organization. (2022). Coronavirus disease 2019 (COVID-19): WHO Thailand situation report – 233. https://reliefweb.int/report/thailand/coronavirus-disease-2019-covid-19-who-thailand-situation-report-233-27-april-2022
World Health Organization Thailand. (2022). COVID-19 situation report Thailand. https://www.who.int/countries/tha
Worakunphanich, W., et al. (2021). Safety of Andrographis paniculata: A systematic review and meta-analysis. Pharmacoepidemiology and Drug Safety.
ดาวน์โหลด
เผยแพร่แล้ว
รูปแบบการอ้างอิง
ฉบับ
ประเภทบทความ
สัญญาอนุญาต
ลิขสิทธิ์ (c) 2025 วารสารสาธารณสุขและวิทยาศาสตร์สุขภาพ

อนุญาตภายใต้เงื่อนไข Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
บทความทุกบทความที่ได้รับการตีพิมพ์ถือเป็นลิขสิทธิ์ของ วารสารสาธารณสุข















