ผลของยากลุ่ม SGLT2 inhibitors ต่อระดับกรดยูริกในเลือดและการเกิดโรคเกาต์ในผู้ป่วยโรคเบาหวาน
คำสำคัญ:
SGLT2 inhibitors, ภาวะกรดยูริกในเลือดสูง, โรคเกาต์บทคัดย่อ
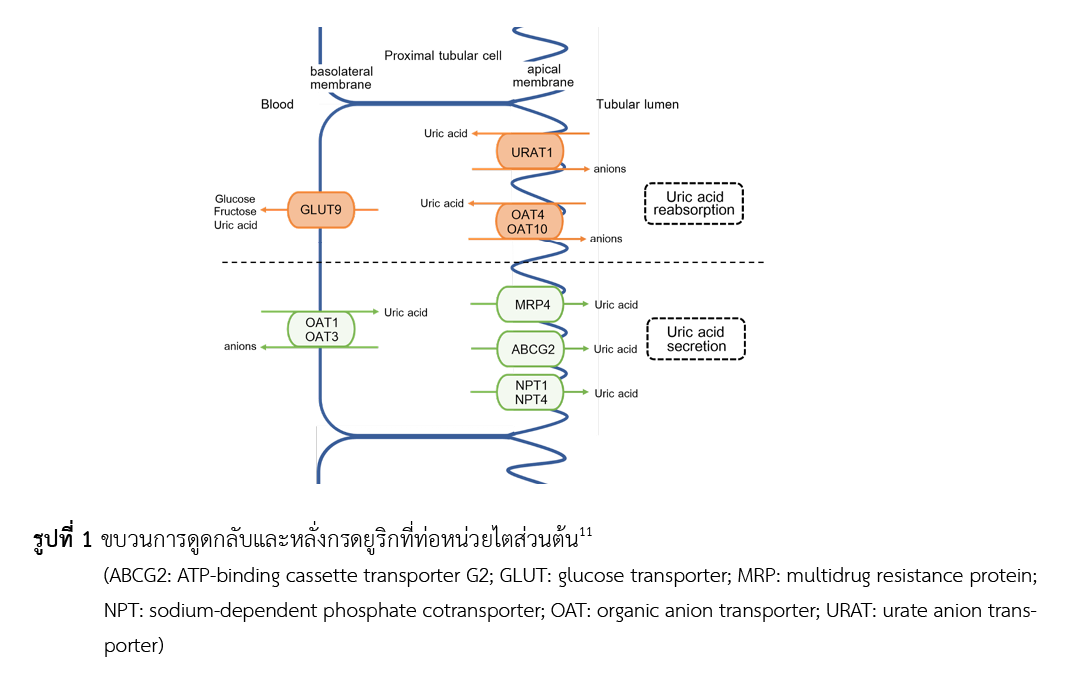
ภาวะกรดยูริกในเลือดสูงเมื่อเป็นติดต่อกันระยะเวลานานจะทำให้เกิดโรคเกาต์ เพิ่มความเสี่ยงต่อการเกิดโรคความดันโลหิตสูงและโรคหัวใจและหลอดเลือด และยังพบภาวะกรดยูริกในเลือดสูงได้บ่อยในผู้ป่วยโรคเบาหวาน ยากลุ่ม sodium-glucose co-transporter 2 (SGLT2) inhibitors เป็นยาชนิดรับประทานที่ใช้รักษาเบาหวานชนิดที่ 2 โดยออกฤทธิ์ยับยั้งโปรตีน SGLT2 ที่ท่อไตส่วนต้น จึงมีผลยับยั้งการดูดกลับของกลูโคสที่ไต ทำให้มีกลูโคสถูกขับออกทางปัสสาวะเพิ่มขึ้น การศึกษาทางคลินิกของยากลุ่ม SGLT2 inhibitors พบว่า สามารถลดระดับกรดยูริกในเลือดและลดความเสี่ยงการเกิดโรคเกาต์ในผู้ป่วยเบาหวานชนิดที่ 2 ได้ โดยคาดว่าเกิดจากปริมาณกลูโคสในปัสสาวะที่สูงขึ้น ไปกระตุ้นให้เกิดการขับกรดยูริกออกทางปัสสาวะเพิ่มขึ้นผ่านทางตัวขนส่ง glucose transporter 9 (GLUT9) isoform 2 จึงมีผลทำให้ปริมาณกรดยูริกในเลือดลดลง ซึ่งเป็นกลไกที่แตกต่างจากยาลดกรดยูริกในปัจจุบัน ดังนั้น ยากลุ่ม SGLT2 inhibitors อาจจะเพิ่มประสิทธิภาพในการลดกรดยูริกในเลือดและลดการเกิดโรคเกาต์ในผู้ป่วยเบาหวานชนิดที่ 2 ได้
เอกสารอ้างอิง
So A, Thorens B. Uric acid transport and disease. J Clin Invest. 2010;120(6):1791-9.
Zhao Y, Xu L, Tian D, Xia P, Zheng H, Wang L, et al. Effects of sodium-glucose co-transporter 2 (SGLT2) inhibitors on serum uric acid level: a meta-analysis of randomized controlled trials. Diabetes Obes Metab. 2018;20(2):458-62.
Ahmadieh H, Azar S. Effects of sodium glucose cotransporter-2 inhibitors on serum uric acid in type 2 diabetes mellitus. Diabetes Technol Ther. 2017;19(9):507-12.
Tat V, Forest CP. The role of SGLT2 inhibitors in managing type 2 diabetes. JAAPA. 2018;31(6):35-40.
Fralick M, Chen SK, Patorno E, Kim SC. Assessing the risk for gout with sodium–glucose cotransporter-2 inhibitors in patients with type 2 diabetes: a population-based cohort study. Ann Intern Med. 2020;172(3):186-94.
Dalbeth N, Merriman TR, Stamp LK. Gout. Lancet. 2016;388(10055):2039-52.
Thai Rheumatism Association. Guideline for management of gout [Internet]: Thai Rheumatism Association; 2012 [cited 2020 Mar 4]. Available from: https://www.thairheumatology.org/.
Merriman T, Dalbeth N. Genetic and environmental risk factors in hyperuricaemia and common gout. Curr Rheumatol Rev. 2011;7:114-22.
Benn CL, Dua P, Gurrell R, Loudon P, Pike A, Storer RI, et al. Physiology of hyperuricemia and urate-lowering treatments. Front Med (Lausanne). 2018;5:160.
Bailey CJ. Uric acid and the cardio-renal effects of SGLT2 inhibitors. Diabetes Obes Metab. 2019;21(6):1291-8.
Stewart DJ, Langlois V, Noone D. Hyperuricemia and hypertension: links and risks. Integr Blood Press Control. 2019;12:43-62.
Ben Salem C, Slim R, Fathallah N, Hmouda H. Drug-induced hyperuricaemia and gout. Rheumatology (Oxford). 2017;56(5):679-88.
Khanna D, Fitzgerald JD, Khanna PP, Bae S, Singh MK, Neogi T, et al. 2012 American College of Rheumatology guidelines for management of gout. Part 1: systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia. Arthritis Care Res (Hoboken). 2012;64(10):1431-46.
Micromedex® (2020). IBM Watson Health, Greenwood Village, Colorado, USA. [cited 2020 Mar 8]. Available from: https://www.micromedexsolutions.com/.
U.S. Food and Drug Administration. FDA adds boxed warning for increased risk of death with gout medicine Uloric (febuxostat) [Internet]: U.S. Food and Drug Administration; 2019 [cited 2020 Mar 10]. Available from: https://www.fda.gov/.
Wolff ML, Cruz JL, Vanderman AJ, Brown JN. The effect of angiotensin II receptor blockers on hyperuricemia. Ther Adv Chronic Dis. 2015;6(6):339-46.
Waldman B, Ansquer JC, Sullivan DR, Jenkins AJ, McGill N, Buizen L, et al. Effect of fenofibrate on uric acid and gout in type 2 diabetes: a post-hoc analysis of the randomised, controlled FIELD study. Lancet Diabetes Endocrinol. 2018;6(4):310-8.
Dalbeth N, Stamp L. Hyperuricaemia and gout: time for a new staging system? Ann Rheum Dis. 2014;73(9):1598-600.
Mortada I. Hyperuricemia, type 2 diabetes mellitus, and hypertension: an emerging association. Curr Hypertens Rep. 2017;19(9):69.
Abeles AM. Hyperuricemia, gout, and cardiovascular disease: an update. Curr Rheumatol Rep. 2015;17(3):13.
Zhao L, Cao L, Zhao TY, Yang X, Zhu XX, Zou HJ, et al. Cardiovascular events in hyperuricemia population and a cardiovascular benefit-risk assessment of urate-lowering therapies: a systematic review and meta-analysis. Chin Med J (Engl). 2020;133(8):982-93.
Wang H, Zhang H, Sun L, Guo W. Roles of hyperuricemia in metabolic syndrome and cardiac-kidney-vascular system diseases. Am J Transl Res. 2018;10(9):2749-63.
Wang J, Chen RP, Lei L, Song QQ, Zhang RY, Li YB, et al. Prevalence and determinants of hyperuricemia in type 2 diabetes mellitus patients with central obesity in Guangdong Province in China. Asia Pac J Clin Nutr. 2013;22(4):590-8.
Arersa KK, Wondimnew T, Welde M, Husen TM. Prevalence and determinants of hyperuricemia in type 2 diabetes mellitus patients attending Jimma Medical Center, Southwestern Ethiopia, 2019. Diabetes Metab Syndr Obes. 2020;13:2059-67.
Lv Q, Meng XF, He FF, Chen S, Su H, Xiong J, et al. High serum uric acid and increased risk of type 2 diabetes: a systemic review and meta-analysis of prospective cohort studies. PLoS One. 2013;8(2):e56864.
Hsia DS, Grove O, Cefalu WT. An update on sodium-glucose co-transporter-2 inhibitors for the treatment of diabetes mellitus. Curr Opin Endocrinol Diabetes Obes. 2017;24(1):73-9.
Lupsa BC, Inzucchi SE. Use of SGLT2 inhibitors in type 2 diabetes: weighing the risks and benefits. Diabetologia. 2018;61(10):2118-25.
Lytvyn Y, Škrtić M, Yang GK, Yip PM, Perkins BA, Cherney DZI. Glycosuria-mediated urinary uric acid excretion in patients with uncomplicated type 1 diabetes mellitus. Am J Physiol Renal Physiol. 2015;308(2):F77-F83.
Chino Y, Samukawa Y, Sakai S, Nakai Y, Yamaguchi J-i, Nakanishi T, et al. SGLT2 inhibitor lowers serum uric acid through alteration of uric acid transport activity in renal tubule by increased glycosuria. Biopharm Drug Dispos. 2014;35(7):391-404.
Xin Y, Guo Y, Li Y, Ma Y, Li L, Jiang H. Effects of sodium glucose cotransporter-2 inhibitors on serum uric acid in type 2 diabetes mellitus: a systematic review with an indirect comparison meta-analysis. Saudi J Biol Sci. 2019;26(2):421-6.
Hao Z, Huang X, Shao H, Tian F. Effects of dapagliflozin on serum uric acid levels in hospitalized type 2 diabetic patients with inadequate glycemic control: a randomized controlled trial. Ther Clin Risk Manag. 2018;14:2407-13.
Li J, Badve SV, Zhou Z, Rodgers A, Day R, Oh R, et al. The effects of canagliflozin on gout in type 2 diabetes: a post-hoc analysis of the CANVAS program. Lancet Rheumatol. 2019;1(4):e220-e8.
Tanaka M, Yamakage H, Inoue T, Odori S, Kusakabe T, Shimatsu A, et al. Beneficial effects of ipragliflozin on the renal function and serum uric acid levels in Japanese patients with type 2 diabetes: a randomized, 12-week, open-label, active-controlled trial. Intern Med. 2020;59(5):601-9.
Filippas-Ntekouan S, Filippatos TD, Elisaf MS. SGLT2 inhibitors: are they safe? Postgrad Med. 2018;130(1):72-82.
U.S. Food and Drug Administration. FDA warns about rare occurrences of a serious infection of the genital area with SGLT2 inhibitors for diabetes [Internet]: U.S. Food and Drug Administration; 2018 [cited 2020 Mar 12]. Available from: https://www.fda.gov/.
Bilezikian JP, Watts NB, Usiskin K, Polidori D, Fung A, Sullivan D, et al. Evaluation of bone mineral density and bone biomarkers in patients with type 2 diabetes treated with canagliflozin. J Clin Endocrinol Metab. 2016;101(1):44-51.
ดาวน์โหลด
เผยแพร่แล้ว
รูปแบบการอ้างอิง
ฉบับ
ประเภทบทความ
สัญญาอนุญาต
ข้อความภายในบทความที่ตีพิมพ์ในวารสารเภสัชกรรมโรงพยาบาลทั้งหมด รวมถึงรูปภาพประกอบ ตาราง เป็นลิขสิทธิ์ของสมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) การนำเนื้อหา ข้อความหรือข้อคิดเห็น รูปภาพ ตาราง ของบทความไปจัดพิมพ์เผยแพร่ในรูปแบบต่าง ๆ เพื่อใช้ประโยชน์ในเชิงพาณิชย์ ต้องได้รับอนุญาตจากกองบรรณาธิการวารสาร (สมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย)) อย่างเป็นลายลักษณ์อักษร
สมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) อนุญาตให้สามารถนำไฟล์บทความไปใช้ประโยชน์และเผยแพร่ต่อได้ โดยอยู่ภายใต้เงื่อนไขสัญญาอนุญาตครีเอทีฟคอมมอน (Creative Commons License: CC) โดย ต้องแสดงที่มาจากวารสาร – ไม่ใช้เพื่อการค้า – ห้ามแก้ไขดัดแปลง, Attribution-NonCommercial-NoDerivatives 4.0 International (CC BY-NC-ND 4.0)
ข้อความที่ปรากฏในบทความในวารสารเป็นความคิดเห็นส่วนตัวของผู้เขียนแต่ละท่านไม่เกี่ยวข้องกับสมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) และบุคลากรในสมาคมฯ แต่อย่างใด ความรับผิดชอบองค์ประกอบทั้งหมดของบทความแต่ละเรื่องเป็นของผู้เขียนแต่ละท่าน หากมีความผิดพลาดใด ๆ ผู้เขียนแต่ละท่านจะรับผิดชอบบทความของตนเอง ตลอดจนความรับผิดชอบด้านเนื้อหาและการตรวจร่างบทความเป็นของผู้เขียน ไม่เกี่ยวข้องกับกองบรรณาธิการ


.png)

