อุบัติการณ์และปัจจัยที่สัมพันธ์กับเหตุการณ์ไม่พึงประสงค์ภายหลังได้รับวัคซีนโรคติดเชื้อไวรัสโคโรนา 2019: การศึกษาเชิงสังเกตนาน 1 ปี
คำสำคัญ:
วัคซีนโรคติดเชื้อไวรัสโคโรนา 2019, วัคซีนโควิด 19, เหตุการณ์ไม่พึงประสงค์ภายหลังได้รับวัคซีนโควิด 19บทคัดย่อ
ความสำคัญ: วัคซีนโรคติดเชื้อไวรัสโคโรนา 2019 (วัคซีนโควิด-19) ถูกพัฒนาขึ้นในภาวะฉุกเฉินเพื่อลดความรุนแรงของโรค ซึ่งควรเฝ้าระวังการเกิดเหตุการณ์ไม่พึงประสงค์
วัตถุประสงค์: เพื่อรวบรวมเหตุการณ์ไม่พึงประสงค์และวิเคราะห์ปัจจัยที่สัมพันธ์กับการเกิดเหตุการณ์ไม่พึงประสงค์ภายหลังการได้รับวัคซีนโควิด 19
วิธีวิจัย: งานวิจัยนี้เป็นการศึกษาเชิงสังเกตโดยเก็บข้อมูลเหตุการณ์ไม่พึงประสงค์จากระบบรายงานของกระทรวงสาธารณสุข และ spontaneous report ของโรงพยาบาลสุราษฎร์ธานี ในผู้ที่ได้รับวัคซีนโควิด-19 จากศูนย์ฉีดวัคซีนโรงพยาบาลสุราษฎร์ธานีในช่วงระหว่างวันที่ 10 เมษายน 2564 ถึง 30 เมษายน 2565 วิเคราะห์ข้อมูลทั่วไปโดยใช้สถิติเชิงพรรณนา วิเคราะห์ความแตกต่างของเหตุการณ์ไม่พึงประสงค์จากวัคซีนแต่ละชนิดโดยใช้ Chi-square หรือ Fisher’s exact test และวิเคราะห์ปัจจัยที่สัมพันธ์กับการเกิดเหตุการณ์ไม่พึงประสงค์ โดย multiple logistic regression
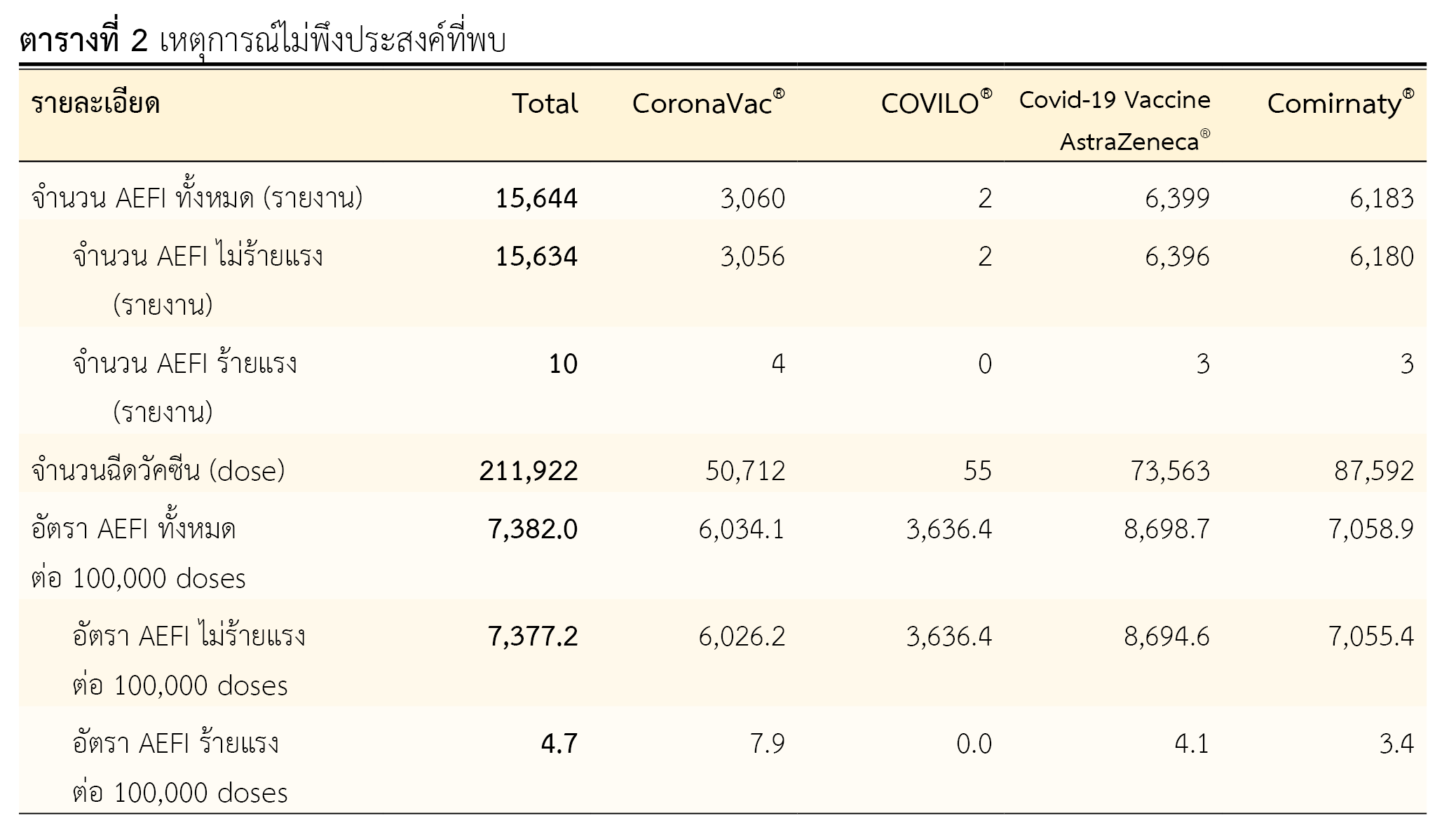
ผลการวิจัย: ในช่วงเวลาที่ศึกษามีการฉีดวัคซีนโควิด-19 ในประชากร 113,570 คน รวมทั้งหมด 211,922 dose พบรายงานเหตุการณ์ไม่พึงประสงค์ภายหลังได้รับการสร้างเสริมภูมิคุ้มกันโรคจำนวน 15,644 รายงาน เป็นอาการไม่ร้ายแรง 15,634 รายงาน และอาการร้ายแรง 10 รายงาน วัคซีนโควิด-19 ที่มีรายงานเหตุการณ์ไม่พึงประสงค์จากวัคซีนมากที่สุดคือ Covid-19 Vaccine AstraZeneca® 6,399 รายงาน เหตุการณ์ไม่พึงประสงค์ชนิดร้ายแรง ได้แก่ ภูมิแพ้เฉียบพลันรุนแรง 3 รายงาน กล้ามเนื้อหัวใจตาย 3 รายงาน เยื่อหุ้มหัวใจอักเสบเฉียบพลัน 2 รายงาน กล้ามเนื้อและเยื่อหุ้มหัวใจอักเสบ 1 รายงาน และสมองอักเสบ 1 รายงาน ปัจจัยที่สัมพันธ์กับการเกิดเหตุการณ์ไม่พึงประสงค์จากการศึกษาได้แก่ อายุ เพศ ชนิดวัคซีนและโรคประจำตัว กลุ่มอายุมากกว่าหรือเท่ากับ 60 ปี เพิ่มโอกาสเกิดกลุ่มอาการหัวใจและหลอดเลือด กลุ่มอายุน้อยกว่า 18 ปี และ 18-29 ปี เพิ่มโอกาสเกิดกลุ่มอาการทางระบบประสาท และเพศหญิงเกิดอาการไม่พึงประสงค์ที่หลากหลายกว่าเพศชาย เหตุการณ์ไม่พึงประสงค์มักสัมพันธ์กับโรคประจำตัวเดิม ในกลุ่มที่เกิดอาการร้ายแรงมักจะมีโรคประจำตัวร่วมด้วย
สรุปผล: เหตุการณ์ไม่พึงประสงค์ภายหลังได้รับการสร้างเสริมภูมิคุ้มกันโรคด้วยวัคซีนโควิด-19 ส่วนใหญ่มาจาก Covid-19 Vaccine AstraZeneca® และเป็นอาการไม่ร้ายแรง อายุ เพศ ชนิดวัคซีน และ โรคประจำตัว มีความสัมพันธ์กับการเกิดเหตุการณ์ไม่พึงประสงค์ภายหลังได้รับการสร้างเสริมภูมิคุ้มกันโรค
เอกสารอ้างอิง
กรมควบคุมโรค. แนวทางการให้วัคซีนโควิด 19 ในสถานการณ์การระบาด ปี 2564 ของประเทศไทย ฉบับปรับปรุง ครั้งที่ 2 [อินเทอร์เน็ต]. นนทบุรี: กรมควบคุมโรค กระทรวงสาธารณสุข; 2564 [สืบค้นเมื่อ 7 กรกฎาคม 2565]. สืบค้นจาก: https://ddc.moph.go.th/vaccine-covid19/getFiles/11/1628849610213.pdf
World Health Organization. WHO Coronavirus (COVID-19) Dashboard [Internet]. n.p.: World Health Organization; 2022 [cited 2022 Oct 15]. Available from: https://covid19.who.int/
กรมควบคุมโรค. สถานการณ์ผู้ติดเชื้อ COVID-19 ภายในประเทศ [อินเทอร์เน็ต]. นนทบุรี: กรมควบคุมโรค กระทรวงสาธารณสุข; 2565 [สืบค้นเมื่อ 15 ตุลาคม 2565]. สืบค้นจาก: https://ddc.moph.go.th/covid19-dashboard/
World Health Organization. The different types of COVID-19 vaccines [Internet]. Geneva: World Health Organization; 2022 [cited 2022 Jul 7]. Available from: https://www.who.int/news-room/feature-stories/detail/the-race-for-a-covid-19-vaccine-explained
Centers for Disease Control and Prevention. Safety of COVID-19 vaccines [Internet]. n.p.: Centers for Disease Control and Prevention; 2022 [cited 2022 Jul 10]. Available from: https://www.cdc.gov/coronavirus/2019-ncov/vaccines/safety/safety-of-vaccines.html
Chen M, Yuan Y, Zhou Y, Deng Z, Zhao J, Feng F, et al. Safety of SARS-CoV-2 vaccines: a systematic review and meta‑analysis of randomized controlled trials. Infect Dis Poverty. 2021;10(1):94. doi: 10.1186/s40249-021-00878-5.
Singh A, Khillan R, Mishra Y, Khurana S. The safety profile of COVID-19 vaccinations in the United States. Am J Infect Control. 2022; 50(1):15-9. doi: 10.1016/j.ajic.2021.10.015.
Tran VN, Nguyen HA, Le TTA, Truong TT, Nguyen PT, Nguyen TTH. Factors influencing adverse events following immunization with AZD1222 in Vietnamese adults during first half of 2021. Vaccine. 2021; 39(44):6485-91. doi: 10.1016/j.vaccine.2021.09.060.
ศูนย์ข้อมูลข่าวสารด้านเวชภัณฑ์ กระทรวงสาธารณสุข. แนวทางการเฝ้าระวังและตอบโต้เหตุการณ์ไม่พึงประสงค์ภายหลังได้รับการสร้างเสริมภูมิคุ้มกันโรคของประเทศไทย [อินเทอร์เน็ต]. นนทบุรี: ศูนย์ข้อมูลข่าวสารด้านเวชภัณฑ์ กระทรวงสาธารณสุข; 2563 [สืบค้นเมื่อ 8 กรกฎาคม 2565]. สืบค้นจาก: http://dmsic.moph.go.th/index/detail/8388กรมควบคุมโรค
กรมควบคุมโรค กองระบาดวิทยา. แนวทางการเฝ้าระวังและสอบสวนเหตุการณ์ไม่พึงประสงค์ภายหลังได้รับวัคซีนป้องกันโรคโควิด-19 [อินเทอร์เน็ต]. นนทบุรี: กรมควบคุมโรค; 2564 [สืบค้นเมื่อ 8 กรกฎาคม 2565]. สืบค้นจาก: https://apps-doe.moph.go.th/boe/software/file/Guideline_AEFI_COVID19vaccine_DOE_17062021.pdf
Ontario Agency for Health Protection and Promotion (Public Health Ontario). Adverse events following immunization (AEFIs) for COVID-19 in Ontario: December 13, 2020 to January 29, 2023 [Internet]. Toronto, ON: Queen’s Printer for Ontario; 2023 [cited 2023 Feb 24]. Available from: https://www.publichealthontario.ca/-/media/Documents/nCoV/Archives/AEFI/2023/02/covid-19-aefi-report-2023-02-03.pdf?rev=55a0cf1dc6554e5fb643d6c1089c9da3&sc_lang=en
Bouman A, Schipper M, Heineman MJ, Faas MM. Gender difference in the non-specific and specific immune response in humans. Am J Reprod Immunol. 2004;52(1):19-26. doi: 10.1111/j.1600-0897.2004.00177.x.
Tomita K, Okada S, Sugihara S, Ikeuchi T, Touge H, Hasegawa J, et al. Physical characteristics of injection site pain after COVID-19 mRNA BNT162b2 vaccination. Yonago Acta Med. 2021; 64(4): 339–44. doi: 10.33160/yam.2021.11.003.
ดาวน์โหลด
เผยแพร่แล้ว
รูปแบบการอ้างอิง
ฉบับ
ประเภทบทความ
สัญญาอนุญาต
ลิขสิทธิ์ (c) 2023 สมาคมเภสัชกรรมโรงพยาบาล(ประเทศไทย)

อนุญาตภายใต้เงื่อนไข Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
ข้อความภายในบทความที่ตีพิมพ์ในวารสารเภสัชกรรมโรงพยาบาลทั้งหมด รวมถึงรูปภาพประกอบ ตาราง เป็นลิขสิทธิ์ของสมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) การนำเนื้อหา ข้อความหรือข้อคิดเห็น รูปภาพ ตาราง ของบทความไปจัดพิมพ์เผยแพร่ในรูปแบบต่าง ๆ เพื่อใช้ประโยชน์ในเชิงพาณิชย์ ต้องได้รับอนุญาตจากกองบรรณาธิการวารสาร (สมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย)) อย่างเป็นลายลักษณ์อักษร
สมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) อนุญาตให้สามารถนำไฟล์บทความไปใช้ประโยชน์และเผยแพร่ต่อได้ โดยอยู่ภายใต้เงื่อนไขสัญญาอนุญาตครีเอทีฟคอมมอน (Creative Commons License: CC) โดย ต้องแสดงที่มาจากวารสาร – ไม่ใช้เพื่อการค้า – ห้ามแก้ไขดัดแปลง, Attribution-NonCommercial-NoDerivatives 4.0 International (CC BY-NC-ND 4.0)
ข้อความที่ปรากฏในบทความในวารสารเป็นความคิดเห็นส่วนตัวของผู้เขียนแต่ละท่านไม่เกี่ยวข้องกับสมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) และบุคลากรในสมาคมฯ แต่อย่างใด ความรับผิดชอบองค์ประกอบทั้งหมดของบทความแต่ละเรื่องเป็นของผู้เขียนแต่ละท่าน หากมีความผิดพลาดใด ๆ ผู้เขียนแต่ละท่านจะรับผิดชอบบทความของตนเอง ตลอดจนความรับผิดชอบด้านเนื้อหาและการตรวจร่างบทความเป็นของผู้เขียน ไม่เกี่ยวข้องกับกองบรรณาธิการ


.png)

