A Assessment Study of Trigger for Detecting Nephrotoxicity from Tenofovir Disoproxil Fumarate
Keywords:
adverse effect detection, nephrotoxicity, tenofovir, trigger toolAbstract
Background: Tenofovir-induced nephrotoxicity is detected from eGFR, urine glucose, proteinuria, serum potassium, and urine phosphate. Serum phosphorus is another standard diagnosis. Unfortunately, some patients are not investigated for this latter test as it is not included in the Universal Coverage benefit package of National Health Security Office.Objective: To develop a monitoring system that includes a trigger tool and evaluate its effectiveness in detecting tenofovir-induced nephrotoxicity.
Method: Part 1 A retrospective analysis was performed on data from a database between January 2020 and December 2021. The effectiveness of the trigger was calculated based on its sensitivity, specificity, positive predictive value, negative predictive value, and accuracy. Part 2 A focus group of an HIV clinic's interdisciplinary team was used to gather consensus on workflow improvement.
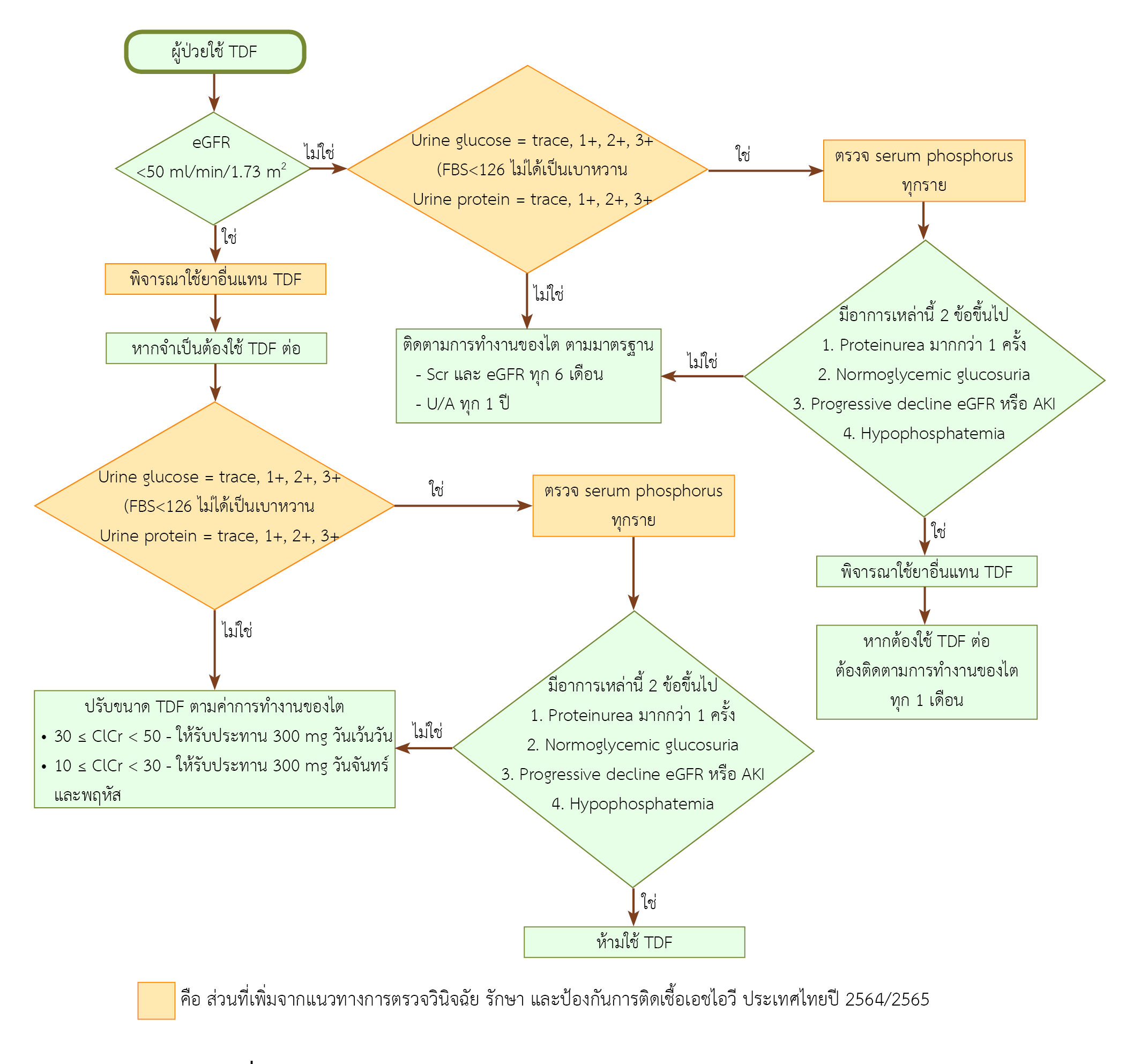
Result: Among 1,059 visits, 6.98% of them involved tenofovir-induced nephrotoxicity. Serum phosphorus functions as the best trigger. When this trigger was used along with eGFR and urine sugar, the efficiency of trigger tools is 100%. The focus group resulted in the development of a procedure for monitoring serum phosphorus levels in all patients whose tested positive for proteinuria or sugar in the urine.
Conclusion: Urine sugar, eGFR, and serum phosphorus, all can be used to detect tenofovir-induced nephrotoxicity. The workflow for monitoring tenofovir-induced nephrotoxicity has been developed through interdisciplinary collaboration, and as a consequence, it is straightforward and efficient, which can increase patient safety.
References
UNAIDS. Global HIV & AIDS statistics - fact sheet 2020 [Internet]. Geneva: The Joint United Nations Programme on HIV/AIDS (UNAIDS); 2020 [cited 2022 Jun 30]. Available from: http://www.unaids.org/en/resources/fact-sheet
กรมควบคุมโรค. กองโรคเอดส์และโรคติดต่อทางเพศสัมพันธ์. สรุปสถานการณ์ผู้ป่วยเอดส์และการติดเชื้อเอชไอวีในประเทศไทย 2564 [อินเทอร์เน็ต]. นนทบุรี: กรมควบคุมโรค; 2565 [สืบค้นเมื่อ 30 ต.ค. 2565]. สืบค้นจาก: https://hivhub.ddc.moph.go.th/epidemic.php
Grim SA, Romanelli F. Tenofovir disoproxil fumarate. Ann Pharmacother. 2003;37(6):849-59. doi: 10.1345/aph.1C388.
Gallant JE, Pham PA. Tenofovir disoproxil fumarate (Viread®) for the treatment of HIV infection. Expert Rev Anti Infect Ther. 2003;1(3):415-22. doi: 10.1586/14787210.1.3.415.
เกียรติ รักษ์รุ่งธรรม, กุลกัญญา โชคไพบูลย์กิจ, เพลินจันทร์ เชษฐ์โชติศักดิ์, สุวัฒน์ จริยาเลิศศักดิ์, ศศิโสภิณ เกีรติบูรณกุล, โอภาส พุทธเจริญ, และคณะ. แนวทางการตรวจรักษาและป้องกันการติดเชื้อเอชไอวี ประเทศไทย ปี 2564/2565 [อินเทอร์เน็ต]. นนทบุรี: กองโรคเอดส์และโรคติดต่อทางเพศสัมพันธ์ กรมควบคุมโรค; 2565 [สืบค้นเมื่อ 30 มิ.ย. 2565]. สืบค้นจาก: https://ddc.moph.go.th/uploads/publish/1281020220531045539.pdf
Eggleton JS, Nagalli S. Highly active antiretroviral therapy (HAART). 2022 Jul 4. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023. Available from: https://www.ncbi.nlm.nih.gov/books/NBK554533/
DeJesus E, Haas B, Segal-Maurer S, Ramgopal MN, Mills A, Margot N, et al. Superior efficacy and improved renal and bone safety after switching from a tenofovir disoproxil fumarate- to a tenofovir alafenamide-based regimen through 96 weeks of treatment. AIDS Res Hum Retroviruses. 2018;34(4):337-42. doi: 10.1089/AID.2017.0203.
Hall AM, Hendry BM, Nitsch D, Connolly JO. Tenofovir-associated kidney toxicity in HIV-infected patients: a review of the evidence. Am J Kidney Dis. 2011;57(5):773-80. doi: 10.1053/j.ajkd.2011.01.022.
European AIDS Clinical Society. EACS guidelines version 11.0 October 2021 [Internet]. Brussels: European AIDS Clinical Society (EACS); 2021 [cited 2022 Jun 25]. Available from: https://www.eacsociety.org/media/final2021eacsguidelinesv11.0_oct2021.pdf
Rozich JD, Haraden CR, Resar RK. Adverse drug event trigger tool: a practical methodology for measuring medication related harm. Qual Saf Health Care. 2003;12(3):194-200. doi: 10.1136/qhc.12.3.194.
สถาบันรับรองคุณภาพสถานพยาบาล (องค์การมหาชน). มาตรฐานโรงพยาบาลและบริการสุขภาพ ฉบับที่ 5 [อินเทอร์เน็ต]. พิมพ์ครั้งที่ 2. นนทบุรี: สถาบันรับรองคุณภาพสถานพยาบาล (องค์การมหาชน); 2565 [สืบค้นเมื่อ 31 ส.ค. 2565]. 256 หน้า. สืบค้นจาก: https://www.ha.or.th/TH/Posts/หนังสือการพัฒนาคุณภาพ/Details/132#
Scherzer R, Estrella M, Li Y, Choi AI, Deeks SG, Grunfeld C, et al. Association of tenofovir exposure with kidney disease risk in HIV infection. AIDS 2012;26(7):867–75. doi: 10.1097/QAD.0b013e328351f68f.
Chaisiri K, Bowonwatanuwong C, Kasettratat N, Kiertiburanakul S. Incidence and risk factors for tenofovir-associated renal function decline among Thai HIV-infected patients with low-body weight. Curr HIV Res 2010;8:504–9. doi: 10.2174/157016210793499259.
Papaleo A, Warszawski J, Salomon R, Jullien V, Veber F, Dechaux M, et al. Increased beta-2 microglobulinuria in human immunodeficiency virus-1-infected children and adolescents treated with tenofovir. Pediatr Infect Dis J. 2007;26(10):949-51. doi: 10.1097/INF.0b013e3181256570.
พสุเพ็ญ สุขเกษม, รัตนาภรณ์ อาวิพันธ์, นันทวรรณ กิติกรรณากรณ์. การพัฒนาระบบการจัดการความปลอดภัยยาทีโนโฟเวียร์ ไดโซโพรซิล ฟูมาเรต สำหรับผู้ติดเชื้อเอชไอวี ในโรงพยาบาลคลองหลวง จังหวัดปทุมธานี. วารสารเภสัชศาสตร์อีสาน. 2562;15(3):33-44. doi: 10.14456/ijps.2019.31.
ภูริต ทรงธนนิตย,จินตนา ขาวทับ,วิสุทธิ์ กังวานตระกูล,ศิริพร ปรุงวิทยา, ลิ่มทอง พรหมดี. ผลเปรียบเทียบคาประมาณอัตรากรองของไตระหวางสูตร MDRD และ CG ที่ 60 ml/min เทียบกับคายูเรียไนโตรเจน ครีอะตินีน และอัลบูมินในปสสาวะในผูปวยเบาหวานชนิดที่2. ศรีนครินทร์เวชสาร [อินเทอร์เน็ต]. 2558 [สืบค้นเมื่อ 30 มิ.ย. 2565];30(1):19-25. สืบค้นจาก: https://li01.tci-thaijo.org/index.php/SRIMEDJ/article/view/33577
Rutter DR, Bunce DJ. The theory of reasoned action of Fishbein and Ajzen: a test of Towriss's amended procedure for measuring beliefs. Br J Soc Psychol. 1989;28(1):39-46. doi: 10.1111/j.2044-8309.1989.tb00844.x.
Downloads
Published
How to Cite
Issue
Section
License
Copyright (c) 2023 Association of Hospital Pharmacy (Thailand)

This work is licensed under a Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
ข้อความภายในบทความที่ตีพิมพ์ในวารสารเภสัชกรรมโรงพยาบาลทั้งหมด รวมถึงรูปภาพประกอบ ตาราง เป็นลิขสิทธิ์ของสมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) การนำเนื้อหา ข้อความหรือข้อคิดเห็น รูปภาพ ตาราง ของบทความไปจัดพิมพ์เผยแพร่ในรูปแบบต่าง ๆ เพื่อใช้ประโยชน์ในเชิงพาณิชย์ ต้องได้รับอนุญาตจากกองบรรณาธิการวารสาร (สมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย)) อย่างเป็นลายลักษณ์อักษร
สมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) อนุญาตให้สามารถนำไฟล์บทความไปใช้ประโยชน์และเผยแพร่ต่อได้ โดยอยู่ภายใต้เงื่อนไขสัญญาอนุญาตครีเอทีฟคอมมอน (Creative Commons License: CC) โดย ต้องแสดงที่มาจากวารสาร – ไม่ใช้เพื่อการค้า – ห้ามแก้ไขดัดแปลง, Attribution-NonCommercial-NoDerivatives 4.0 International (CC BY-NC-ND 4.0)
ข้อความที่ปรากฏในบทความในวารสารเป็นความคิดเห็นส่วนตัวของผู้เขียนแต่ละท่านไม่เกี่ยวข้องกับสมาคมเภสัชกรรมโรงพยาบาล (ประเทศไทย) และบุคลากรในสมาคมฯ แต่อย่างใด ความรับผิดชอบองค์ประกอบทั้งหมดของบทความแต่ละเรื่องเป็นของผู้เขียนแต่ละท่าน หากมีความผิดพลาดใด ๆ ผู้เขียนแต่ละท่านจะรับผิดชอบบทความของตนเอง ตลอดจนความรับผิดชอบด้านเนื้อหาและการตรวจร่างบทความเป็นของผู้เขียน ไม่เกี่ยวข้องกับกองบรรณาธิการ


.png)

